Вы здесь
Химико-токсикологическое исследование лоразепама
Publication in electronic media: 15.08.2010 under http://journal.forens-lit.ru/node/189
Publication in print media: Актуальные вопросы судебной медицины и экспертной практики, Новосибирск 2009 Вып. 15
Л. Е. Кудрикова, Е. Н. Маскина, Л. Г. Воронкова
г. Барнаул
Смертельные отравления производные 1,4-бензодиазепина довольно часто встречаются в практике судебной химии, особенно в сочетании с этиловым алкоголем, барбитуратами, производными фенотиазина, антигистаминными препаратами.
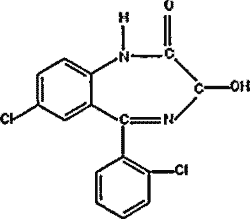
Определенный интерес в практике судебно-химического анализа вызывает лоразепам, методов определения которого в биоматериале, нами в доступной литературе не найдено. Лоразепам (7-Хлор-5-(орто-хлорфенил)-2,3-дигидро-3-окси-1Н-1,4-бензодиазепин-2-OH) применяется под названиями: Апо-Лоразепам, Калмезе, Лорам и др.. Препарат оказывает анксиолитическое, седативное, снотворное, противосудорожное, центральное миорелаксирующее, противорвотное действие. Стабилизирует вегетативную нервную систему.
В настоящее время выделяют два основных направления в анализе биологических объектов на производные 1,4-бензодиазепина: по продуктам гидролиза — аминобензофенонам и по нативным соединениям.
Первое направление включает в себя три основных этапа: кислотный гидролиз биологических объектов, экстракцию аминобензофенонов после подщелачивания органическими растворителями, очистку и анализ экстрактов. Основное преимущество исследования препаратов по производным состоит в том, что данный способ позволяет суммарно определять нативное соединение и ряд его метаболитов в виде бензофенонов. Недостатком является тот факт, что ряд соединений образуют одинаковые бензофеноны и идентификация препарата невозможна.
Второе, более сложное направление, включает изолирование нативных соединений методами экстракции или сорбции. Для биологических жидкостей используется прямая экстракция органическими растворителями из щелочной среды. Для изолирования из внутренних органов могут применяться различные методы. В настоящей работе нами апробирован метод изолирования нейтральным ацетоном по Карташову. Далее для обнаружения и количественного определения производных бензодиазепина и их метаболитов используется комплекс аналитических методов.
Цель работы—оценка метода изолирования лоразепама нейтральным ацетоном по В. А. Карташову с соавт. (1988) и выбор подходящих методов исследования извлечений, проверка разработанной методики анализа в эксперименте на животных.
Методы исследования. Предварительный метод—ТСХ. В качестве основного метода обнаружения и количественного определения лоразепама и продукта его гидролиза нами была выбрана высокоэффективная жидкостная хроматография (ВЭЖХ), которая обладает достаточно высокой чувствительностью и специфичностью. Исследовали спиртовые растворы препаратов производных 1,4-бензодиазепина с концентрацией 200 мкг/мл. Хроматографирование проводили на приборе Милихром А-02, колонка 2x75 мм, dp = 5 мкм, неподвижная фаза — ProntoSil C-18. Растворы препаратов хроматографировали в градиентном режиме: элюент А — вода, элюент В — ацетонитрил. Концентрация ацетонит-рила увеличивалась от 30 до 100% за 15 мин. Скорость подачи элюента 100 мкл/мин. Идентифицировали препараты по временам удерживания и спектральным отношениям. Время удерживания лоразепама составило 7,0 минут. Результаты представлены в таблице 1.
Таблица 1
Результаты исследования препаратов производных 1,4-бензодиазепина методом ВЭЖХ
| Препарат | Время удерживания, мин | Спектральные отношения | |
| D254нм/ D220нм | D300нм/ D220нм | ||
| Клоназепам | 7,5 | 0,5 | * 0,4 |
| Нозепам | 6,7 | 0,5 | 0,1 |
| Седуксен | 5,8 | 0,6 | 0,1 |
| Элениум | 9 | 2 | 0,5 |
| Феназепам | 8,5 | 0,4 | 0 |
| Лоразепам | 7 | 0,5 | 0,4 |
Растворы бензофенонов, которые получены при кислотном гидролизе, хроматографировали в аналогичных условиях, но градиентный режим был другим: концентрация ацетонитрила в элюенте увеличивалась от 50 до 100% за 15 минут. Время удерживания бензофенона лоразепама составило 7,7 минут. Результаты хроматографирования представлены в таблице 2.
Таблица 2
Результаты исследования бензофенонов производных 1,4-бензодиазепина методом ВЭЖХ
| Бензофенон препарата | Время удерживания, мин | Спектральные отношения | ||
| D254нм/ D220нм | D300нм/ D220нм | D360нм/ D220нм | ||
| Клоназепам | 6,1 | - | - | - |
| Нозепам | 7,5 | 0,9 | 0 | 0,2 |
| Седуксен | 8 | 0,1 | 0 | 0,1 |
| Элениум | 7,5 | 0,9 | 0 | 0,2 |
| Феназепам | 9,8 | 0,4 | 0 | 0,2 |
| Лоразепам | 7,7 | 0,4 | 0 | 0,2 |
Спектр 2-амино-5,2'-дихлорбензофенона (продукта гидролиза лоразепама) представлен на рис. 1.
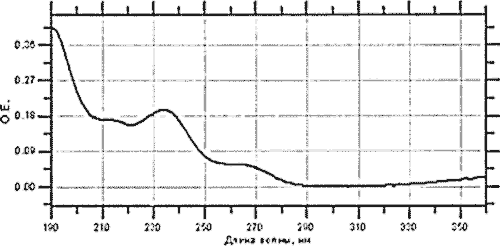
Рис. 1. Спектр продукта гидролиза лоразепама
Максимумы поглощения наблюдаются при длинах волн 233 и 266 нм, что соответствует литературным данным (Еремин С. К. с соавт., 1993).
Из данных приведенных в таблице 2 можно сделать вывод, что выбранные условия хроматографирования позволяют идентифицировать лоразепам и его бензофенон в присутствии других производных 1,4-бензодиазепина и продуктов их гидролиза, а также лоразепам и его бензофенон при совместном присутствии, так как времена удерживания и спектральные отношения отличаются от показателей других бенздиазепинов.
Изолирование и очистка. Изолирование лоразепама из биологического материала (ткань печени) проводили с помощью нейтрального ацетона по методике, описанной В. А. Карташовым с соавт. (1988). Ввиду того, что препарат обладает амфотерным характером, на исследование брали извлечения, как из кислой, так и из щелочной среды. Извлечения из кислой и щелочной среды делили на две части и исследовали методом ВЭЖХ, одну часть — без очистки, другую часть — после очистки методом тонкослойной хроматографии (ТСХ). Результаты исследования представлены в таблице 3.
Таблица 3
Концентрация лоразепама при изолировании нейтральным ацетоном из кислой и щелочной среды без очистки и после очистки
| Опыт | В экстракте из кислой средыв % | В экстракте из щелочной средыв % | ||
| Без очистки | После ТСХ | Без очистки | После ТСХ | |
| 1 | 8,3 | 3,7 | 41,2 | 15,5 |
| 2 | 14,6 | 6,8 | 37,6 | 16,3 |
| 3 | 14,8 | 6,6 | 33,9 | 16,7 |
| Среднее значение | 12,7 | 5,7 | 37,6 | 16,2 |
Из таблицы 3 следует, что наиболее эффективно исследование суммы извлечений без очистки. Очистка извлечений на ТСХ приводит к значительным потерям исследуемых веществ.
Исследование биологического материала по продуктам гидролиза. Гидролиз лоразепама проводили в течение 60 минут, в качестве экстрагента использовали гексан. Экстракты исследовали методом ВЭЖХ, в приведенных ранее условиях. В результате на хроматограмме обнаружены два пика с временами удерживания 7,7 и 8,5 минут. Основываясь на данных о времени удерживания (7,7 минут) и спектральных отношениях сделали вывод, что первый пик принадлежит бензофенону лоразепама.
При хроматографировании извлечений холостого опыта пиков, мешающих определению исследуемых веществ, не было обнаружено.
Проверка методики в эксперименте на животных. Крысе с помощью зонда в желудок ввели водную суспензию таблеток лоразепама, содержащую 30 мг действующего вещества. Через 1,5 часа крысу усыпили эфиром. Для проведения анализа у животного были взяты печень и желудок с содержимым. Одну половину органов исследовали по нативному веществу с использованием ацетонового метода изолирования, другую — взяли для исследования методом кислотного гидролиза. В извлечении из печени был обнаружен пик со временем удерживания (7,02 минуты), что соответствует лоразепаму. Выход нативного вещества из кислой среды составил 4,94 мкг%, из щелочной среды — 5,76 мкг%. В результате анализа извлечений из желудка также был обнаружен лоразепам, выход которого из кислой среды составил 82,44 мкг%, из щелочной — 90 мкг%.
Результаты ВЭЖХ исследования были подтверждены анализом извлечений методом ТСХ. Пятна обнаруживали путем последовательной обработки пластинки раствором ртути сульфата и дифенилкарбазо-на. При обработке хроматограмм реактивом Браттона-Маршала красных пятен не наблюдали, что свидетельствует об отсутствии в извлечении бензофенонов. При исследовании извлечений из желудка методом ТСХ, получились аналогичные результаты — обнаружилось нативное вещество, бензофенон не был обнаружен.
При исследовании биологических объектов методом кислотного гидролиза в извлечении из печени было обнаружено два пика, времена удерживания которых составили 7,7минут- бензофенон и 8,5 минут- побочный продукт гидролиза. При исследовании извлечения из желудка были обнаружены те же два вещества.
При исследовании гидролизатов из печени методом ТСХ на хроматограмме реакцией Браттона-Маршала, проявлялись ярко-оранжевые пятна, что свидетельствует о наличии бензофенонов, нативное вещество не было обнаружено.
Таким образом, лоразепам нативный и его бензофеноны можно извлечь из биоматериала нейтральным ацетоном по В.А.Карташову с последующей идентификацией методами ТСХ и ВЭЖХ.

