Вы здесь
О возможности генетической детерминированности болезни Такаясу
Publication in electronic media: 24.05.2009 under http://journal.forens-lit.ru/node/30
Publication in print media: Актуальные вопросы судебной медицины и экспертной практики, Барнаул-Новосибирск 2008 Вып. 14
г. Салехард
Одним из наиболее актуальных вопросов современной медицины является генетическая предрасположенность заболеваний с поражением соединительной ткани, которая широко обсуждается как в научных кругах, так и в практическом здравоохранении, в частности – в судебно-медицинской практике.
До сих пор нет четкого определения неспецифического аортоартериита. Не только клиницисты, но и мифологи определяли болезнь по имени авторов, впервые описавшие данную патологию (болезнь Такаясу, Марторелля), другие – по представлению процесса как воспалительного с обязательным указанием топографии (локализации) и конечной стадии («облитерация супрааортальных ветвей»), «облитерация артериальных ветвей дуги аорты», «облитерирующий аортит» (Huchard), подключично-каротидный облитерирующий тромбоартериит (Martorell), «облитерирующий брахиоцефальный артериит» (Ask – Upmark), артериит молодых женщин.
Некоторые исследователи предлагают термины «обратная коарктация», «обратный синдром Лериша», «органический стеноз перешейка аорты». Со второй половины ХХ века наиболее предлагаемыми терминами были: «панартериит аорты и ее ветвей», или «панаортоартериит».
Данное многообразие предлагаемой терминологии не отражало сущность этиопатологического процесса, тем более, что многие предлагаемые термины подходили не под один десяток болезней и синдромов, этим создавалась терминологическая неопределенность как для клиницистов, так и для морфологов.
Термин «неспецифический артериит» (собственно и есть болезнь Такаясу), предложенный М.А. Голосовским (1968, 1972), является наиболее узко определяющим патоморфологию нозологического процесса. Клинические проявления и макроскопические исследования известны со времен Веллизия (1664).
В СССР первое сообщение о наблюдении болезни Такаясу принадлежит Н.В. Антелаевой. Если к 1964 г. насчитывалось около 250 работ, то в настоящее время (в основном благодаря результатам работам сосудистых хирургов) известны более 1000. Однако, в настоящее время этиология заболевания недостаточна ясна. Многие исследователи связывают развитие заболевания с возникновением хронического иммунокомплексного воспаления.
В нашей практике имели место два случая разрыва надклапанной части дуги аорты у женщины 1985 г.р. и мужчины 1982 г.р. (являющихся кровными братом и сестрой, умершими в один день с разницей в 2,5 часа). Известно, что их отец умер в молодом возрасте от того же заболевания при подобной клинической картине и морфологии.
Из акта исследования трупа гр-ки. Г., 1985 гр.: «…Под эпикардом правого предсердия с распространением на переднюю часть дуги аорты, надклапанную ее часть, кровоизлияние вишнево-красного цвета… Определяется разрыв аорты, надклапанной ее части, почти полный, за исключением небольшого, шириной 0,5 см. отрезка задней стенки. По краям разрыва определяется отслоение ее интимы на ширину до 1 см. На правой боковой стенки аорты полный разрыв всей стенки длиной 0,8 см, с неровными краями, сообщающиеся с полостью сердечной сорочки. Внутренняя оболочка аорты желтая с множественными атеросклеротическими бляшками хрящевидной консистенции, больше в брюшном отделе, занимающие около 15% поверхности сосуда».
Из акта исследования трупа гр-на. Г., 1982 гр.: «…Сердечная сорочка значительно напряжена, в полости сердечной сорочки около 600 мл крови в виде гладкого блестящего вишнево-красного кровяного свертка. Сердце размерами 13х11х7 см, значительно обложено жиром. Клапанный аппарат сердца и крупных сосудов сформирован правильно. В полостях сердца жидкая кровь… Определяется разрыв интимы надклапанной части дуги аорты в поперечном направлении передней, боковых ее стенок, за исключением задней части, где целостность интимы аорты на протяжении 3 см между концами разрыва сохранена. Края разрыва интимы неровные, по краю разрыва отслоение интимы на ширину до 1,5 см. В области правой боковой стенки аорты, в проекции разрыва интимы, определяется полный разрыв аорты, длиной 3 см с неровными кровоподтечными краями, имеющий сообщение с полостью сердечной сорочки».
При микроскопическом исследовании в обоих случаях нами наблюдалась схожая морфологическая картина патологических изменений: в надклапанной части дуги аорты – выявлено утолщение стенки с крайне выраженными деструктивными изменениями за счет практически полной дезорганизации эластических волокон при окраске по Слинченко с фрагментацией самих волокон и фрагментов распадающейся эластики; пристеночное наложение масс по типу наслаивающихся пластов на стенке интимы; дезорганизация эластики по типу фрагментации (без расслоения волокон эластики по оси длины сосуда); мукоидное набухание и мукоидный некроз фрагментов стенки; очаговое лимфоидно-макрофагальное скопление с началом формирования неспецифического гранулематозного воспаления (рис. 1).
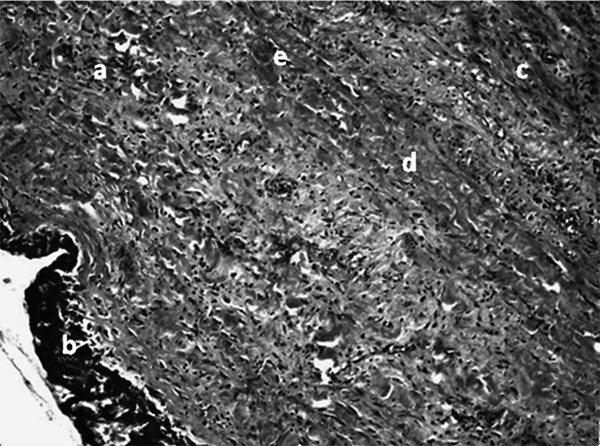 Рис. 1. Фрагмент стенки аорты из области разрыва (интима и часть медии).
Рис. 1. Фрагмент стенки аорты из области разрыва (интима и часть медии).
Буквами обозначено: a) – фрагменты распадающейся эластики; b) – пристеночное наложение масс по типу наслаивающихся пластов на стенке интимы; с) – мукоидное набухание и мукоидный некроз фрагментов стенки; d) – дезорганизация по типу фрагментации, а не расслоения волокон эластики по оси длины сосуда); е) – очаговое лимфоидно-макрофагальное скопление с началом формирования гранулемы.
В толще сосуда диффузная выраженная инфильтрация из лимфоцитов, плазмоцитов (в большом количестве) и макрофагов. Среди воспалительных клеток преобладают плазмоциты. На внутренней поверхности стенки неравномерной толщины наложения бесструктурных масс. Во всех полях зрения очаговые и диффузные кровоизлияния.
На поверхностном слое стенки выраженная лимфоидная, макрофагальная-гистиоидная реакция с большим количеством фибробластов и фиброцитов. Выраженный фибриноидный некроз стенок сосудов аорты с тромбозом просвета. Изменения в стенке аорты носят все стадии воспаления с наличием гранулематозной реакции преимущественно макрофагальной, с выраженным хроническим воспалением в жировой ткани со стороны наружной оболочки, плотно прилегающей к адвентиции, с наличием большого количества новообразованных сосудов в них, с тотальной инфильтрацией лимфоцитами, плазмоцитами, гистиоцитами-макрофагами (без накопления гемосидерина), с наличием тромбоза многих сосудов с фибриноидным некрозом последних, с очаговыми кровоизлияниями без тенденции к слиянию, что не противоречит данным Д.Д. Зербино (1977).
В сердце выявлен диффузно-очаговый серозный миокардит (инфильтрация лимфоцитами, плазмоцитами, макрофагами и единичными лейкоцитами). Выраженный эластоз стенок мелких артериол с дезорганизацией эластических волокон. Острые нарушения микроциркуляции (спазм и дистония артериол, атония капиллярно-венозного русла) и аритмогенные зоны миокарда (мелковолновая, крупноволновая и пилообразная деформация кардиомиоцитов) (рис. 2).
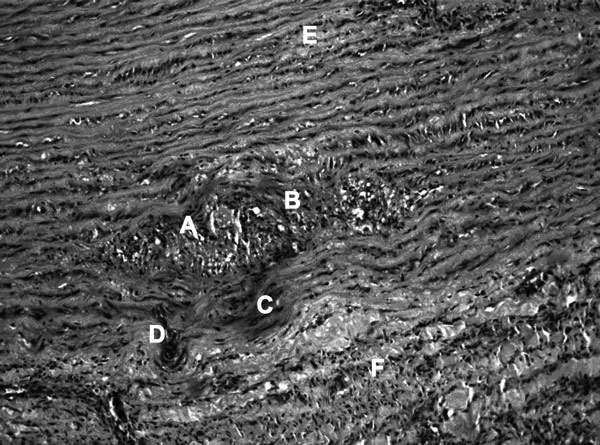 Рис. 2. Часть стенки аорты (основная часть медии до серозной оболочки).
Рис. 2. Часть стенки аорты (основная часть медии до серозной оболочки).
Буквами обозначено: A) – очаговый некроз части стенки с лимфоидно-макрофагальной инфильтрацией, начало формирования волокон фиброзной ткани; B) – новообразованные сосуды по типу капилляров; D) дезорганизация по типу фрагментации, а не расслоения волокон эластики по оси длины сосуда; C) очаговый фибриноидный некроз с зональной воспалительной инфильтрацией; D) – формирование гранулемы;
При болезни Такаясу, неизменными морфологическими проявлениями являются: чередование всех стадий воспаления на фоне уже имеющегося хронического продуктивного неспецифического гранулематозного воспаления с дезорганизацией структуры эластики сосуда артериального типа, с участками некроза ее, с признаками аллергического клеточного компонента, что сочетается с эластозом внутрисердечных артериол.
Таким образом, развитие болезни Такаясу может быть генетически обусловленным. Сам по себе диагноз болезни Такаясу в судебно-медицинской танатологической практике верифицируется не только на макроскопическом описании, но и на основании гистологических дифференциально-диагностических признаков.
Список литературы
1. Зербино Д.Д. Васкулиты и ангиопатии // Киев: «Здоров’я», 1977. – с. 37 – 49.

