Вы здесь
Изолирование карбофурана из биологического материала, его идентификация и количественное определение
Publication in electronic media: 22.10.2011 under http://journal.forens-lit.ru/node/394
Publication in print media: Актуальные вопросы судебной медицины и права, Казань 2010 Вып. 1
ГКУЗ «Республиканское бюро судебно-медицинской экспертизы МЗ РТ»
Карбофуран – О-(2,3-дигидро-2,2-диметил-7-бензофуранил)-N-метилкарба-мат. Эмпирическая формула С12Н15О3N. Молекулярная масса 221,26. Синонимы – фурадан, куратер. Химически чистый карбофуран представляет собой белое кристаллическое вещество с температурой плавления 153-154 °С. Растворимость (при температуре 20 °С) в воде – 700 мг/л, в ацетоне – 150 г/кг, ацетонитриле – 140 г/кг, бензоле – 40 г/кг, диметилсульфоксиде – 270 г/кг, циклогексаноне – 90 г/кг [5]. При комнатной температуре нестабилен в щелочных растворах, стабилен в нейтральных и кислых. Разрушается гипохлоритом кальция [2, 3, 6].
Область применения препарата. Карбофуран – инсектицид и нематоцид системного, контактного и кишечного действия из группы эфиров карбаминовой кислоты. Зарегистрирован в России под торговым названием «фурадан» (текучая паста (350 г/л), используется в качестве инсектицида для рапса, горчицы, а также борьбы с комплексом почвообитающих и наземных вредителей сахарной и кормовой свеклы [2, 5].
Краткая токсикологическая характеристика. Карбофуран относится к чрезвычайно опасным веществам по острой пероральной (ЛД50 для крыс – 8,0 мг/кг, для мышей – 14,4 мг/кг, для собак – 15 мг/кг) [1, 3] и ингаляционной токсичности. Карбофуран обладает значительной токсичностью для теплокровных организмов и относится к 5 классу, а карбофос – к 3 классу токсичности. Кумулятивные свойства выражены слабо. Острое отравление сопровождается симптомами, характерными для действия антихолинэстеразных веществ. Гибель животных наступала в интервале от 10 мин до 4 часов при явлениях паралича дыхания. При однократном введении препарата, меченного С14, установлено, что 40-70% его выводится с мочой и около 3% с фекалиями. Метаболиты: сульфатные и глюкуроновые конъюгаты (в моче), 3-окси-1-глюкуронат (в желчи).
В литературе имеются данные об отравлениях карбофураном людей с летальным исходом [4]. В Татарстане случай отравления карбофураном впервые отмечен в 2009 г. Гражданка Я., 1975 г.р., выпила неизвестную жидкость и скончалась в приемном отделении ЦРБ. На вскрытии отмечено: язык, пищевод, желудок, тонкий кишечник розового цвета.
Для изолирования из биологического материала, затравленного карбофураном, нами были использованы два метода:
- подкисленной водой по Васильевой с последующей экстракцией хло-роформом из кислой среды при рН 2 и из щелочной среды при рН 9 из кон-трольной печени; выход карбофурана из кислой среды составил (61±5)% от добавленного количества, незначительную часть (1,7±0,5)% карбофурана экстрагировали из щелочной среды при рН 9;
- прямое экстрагирование хлористым метиленом из биологических жидкостей, выход карбофурана составил (54±6)% от добавленного количества.
Очистку проводили методом препаративной хроматографии. Аликвоты хлороформного извлечения при рН 2 после испарения растворителя подвергали хроматографированию на пластинках «Сорбфил-ПА» в системе толуол – ацетон (2:1). Участки пластинок, соответствующие зонам карбофурана, элюировали различными элюентами: 1) хлороформ – диэтиловый эфир (2:1); 2) гексан – ацетон (9:1); 3) хлористый метилен. Установлено, что наибольший выход препарата получен при использовании в качестве элюента хлористого метилена (на 15-20% больше, чем при использовании двух первых).
Для хроматографии в тонком слое сорбента на пластинках «Cорбфил-ПА» апробировали несколько систем растворителей (табл. 1).
Таблица 1. Величины Rf в различных системах растворителей
| Величина Rf | |
| 1. Толуол – ацетон (95:5) | 0,45 |
| 2. Гексан - ацетон (3:2) | 0,60 |
| 3. Бензол – этилацетат (13:7) | 0,75 |
Проявление пятен (табл. 2) карбофурана основано на гидролизе препарата спиртовым раствором щелочи и образовании окрашенных соединений с солями диазония: прочный синий Б, прочный голубой Б, прочный красный Б.
Таблица 2. Проявляющие реагенты и окраска пятен
| № пп. | Проявляющие реагенты | Окрашивание |
| 1 | 15% раствор гидроксида калия в спиртово-водном растворе и смесь 0,1% раствора пара-нитроанилина в 0,1 н растворе соляной кислоты и 4% раствора нитрита натрия (10:1) | Красно-вишневое |
| 2 | 15% раствор гидроксида калия в спиртово-водном растворе и 0,01% раствор прочного синего Б в ацетоне | Желтое |
| 3 | Бромфеноловый реактив, нагревание 10 минут при температуре 50 оС и после охлаждения 5% раствор уксусной кислоты | Желтое на фиолетовом фоне |
| 4 | 1% раствор хлорида меди (11) в этиловом спирте | Голубое |
Окраска пятен на пластинке устойчива в течение 1,5 месяцев. При проявлении раствором прочного синего Б метаболиты карбофурана (табл. 3) детектируются пятнами различного цвета [1].
Таблица 3. Окрашивание и флуоресценция пятен карбофурана и его метаболитов
| Карбофуран и метаболиты карбофурана | Флуоресценция в УФ -свете | Окрашивание пятен с прочным синим Б | Величина Rf в системе гексан-ацетон (3:2) |
| Карбофуран | Сиреневая | Желтое | 0,60 |
| О-(2,3-дигидро-2,2-диметил-3-гидрокси-7-бензофу-ранил)-N-метилкарбамат | Желтая | Розовое | 0,38 |
| 2,3-дигидро-2,2-диметил-3,7-бензофурандиол | Фиолетовая | Кирпично-красное | 0,44 |
| 2,3-дигидро-2,2-диметил-3-кето-7-бензофуранил-N-метилкарбамат | Желтая | Сиреневое | 0,49 |
| 2,3-дигидро-2,2-диметил-3-оксо-7-бензофуранол | Желтая | Фиолетовое | 0,59 |
| 2,3-дигидро-2,2-диметил-7-бензофуранол | Оранжевая | Оранжевое | 0,78 |
Сухие остатки аликвот хлороформного извлечения из печени при рН 2 и контрольного раствора карбофурана растворяли в этиловом спирте и снимали спектр поглощения на спектрофотометре НР 8453 «Хьюлетт-Паккард» в интервале длин волн 220-400 нм. Наблюдали максимум поглощения карбофурана при длине волны 276 нм (рис. 1).
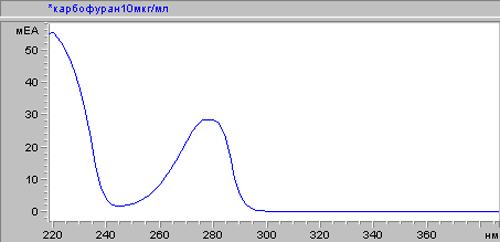
Рис. 1. УФ-спектрограмма карбофурана.
Идентификацию карбофурана (табл. 2) проводили на газовом хроматографе «Кристаллюкс-4000» с использованием пламенно-ионизационного детектора на капиллярной кварцевой колонке длиной 30 м, диаметром 0,32 мм, с нанесенной жидкой фазой OV-101, толщина плёнки жидкой фазы 0,5 мкм. Температура колонки 180 °С, испарителя и детектора 250 °С. Давление газа-носителя (азота) на входе в колонку 1 атм. Скорость воздуха 250 мл/мин, водорода – 30 мл/мин. Время удерживания карбофурана при исследовании стандартного раствора и исследуемых извлечений из кислой среды – 8,11 минуты. В извлечениях регистрировали также пики метаболитов с временем удерживания: 1,35; 2,42; 4,22; 5,59 мин и т.д.
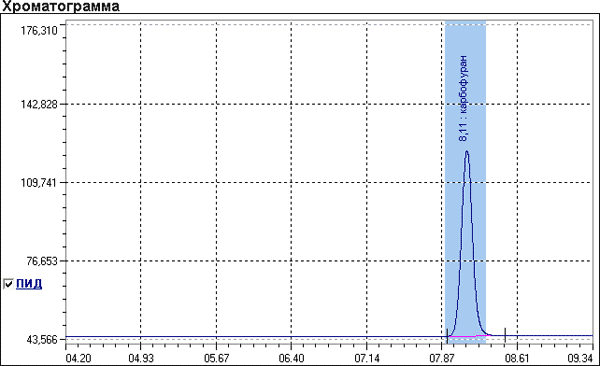
Рис. 2. Хроматограмма ГЖХ исследования карбофурана.
Хромато-масс-спектрометрическое исследование карбофурана проводили на хроматографе «Agilent 6890 Series GC System» с масс-селективным детектором Agilent 5973N на капиллярной кварцевой колонке НР-5MS длиной 30 м, внутренним диаметром 0,25 мм с нанесенной диметилполисилоксановой фазой (толщина пленки фазы 0,25 мкм). Идентификацию компонентов исследуемых образцов проводили по масс-спектрам электронного удара, ионным масс-хроматограммам и библиотекам масс-спектров NIST02.L., WILEY7N.L., ТОХ3.L. На хроматограмме масс-спектрометрически (рис. 3, 4) идентифицировали пик карбофурана (основные ионы m/z = 164, 149, 131, 122, 123, время удерживания - 10,325 мин).
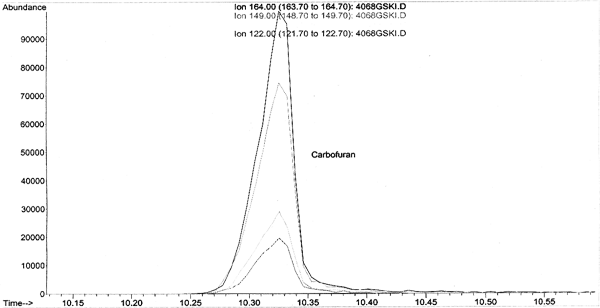
Рис. 3. ХМСС-исследование карбофурана.
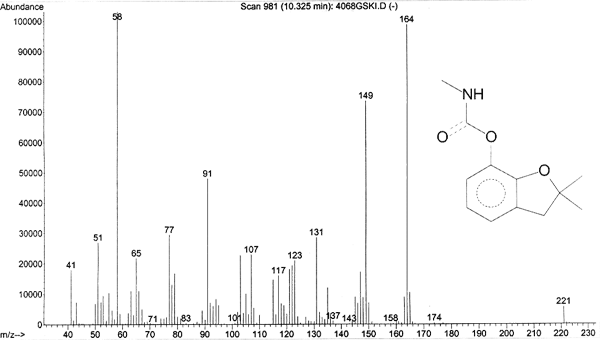
Рис. 4. ХМСС-исследование карбофурана.
Количественное определение карбофурана проводили методом прямой калибровки на высокоэффективном жидкостном хроматографе Agilent Technologies серии 1100 с диодно-матричным детектором. Колонка Hypersil ODS. Подвижная фаза: ацетонитрил-вода (40:60). Скорость потока элюента 1 мл/мл. Рабочая длина волны 278 нм. Объем вводимой пробы 20 мкл. Идентификацию проводили по сопоставлению времен удерживания и УФ спектрам контрольного и исследуемого образцов.
При проведении судебно-химического исследования карбофуран изолировали из желудка подкисленной водой с последующей экстракцией хлороформом при рН 2; из крови и желчи – прямой экстракцией хлористым метиленом. Подтверждена эффективность использованных методов для секционного материала, идентификацию карбофурана и его метаболитов проводили методами газо-жидкостной хроматографии, тонкослойной хроматографии, газовой хроматографии с масс-селективным детектором, высокоэффективной жидкостной хроматографии, спектрофотометрии в УФ-свете. Концентрация карбофурана в крови составила 78 мг/л, в желчи – 3,8 мг/л.
Выводы
- При судебно-химическом исследовании целесообразно проводить изолирование карбофурана из биологических объектов подкисленной водой с последующей экстракцией хлороформом из кислой среды при рН 2; из биологических жидкостей прямой экстракцией хлористым метиленом.
- Для очистки извлечения из биологического материала рекомендуется применение препаративной хроматографии с использованием в качестве элюента хлористого метилена.
- Для идентификации карбофурана и его метаболитов следует применять комплекс физико-химических методов, включающий хроматографию в тонком слое сорбента, высокоэффективную жидкостную хроматографию, газожидкостную хроматографию, хромато-масс-спектрометрию, спектрофотометрию в ультрафиолетовой области спектра. Для количественного определения карбофурана рекомендуется метод высокоэффективной жидкостной хроматографии.
Список литературы
- Вредные вещества в промышленности. Органические вещества // Под редакцией доктора мед. наук Э.Н. Левиной и доктора биол. наук проф. И.Д. Гадаскиной. – Л., 1985. – 221 с.
- Методы определения микроколичеств пестицидов в продуктах питания, кормах и внешней среде. – М., 1992. – Т. 1. – С. 97, 224; Т. 2. – С. 402.
- Определение остаточных количеств карбофурана в воде, почве, корнеплодах, зеленой массе сахарной свеклы, семенах и масле рапса (горчицы) методом газожидкостной хроматографии // Методические указания. МУК 4.1.11392-03 (Утв. главным государственным санитарным врачом РФ 24.06.2003.)
- Справочник по пестицидам // Под ред. проф. А.В. Павлова. – Киев. 1986. – С. 131.
- Справочник по пестицидам // Н.Н. Мельников, К.В. Новожилов и др. –М., 1985. – С. 169.
- Шорманов В.К., Иванов В.П., Королев В.А., Маслов С.В. и др. Судебно-химическое определение фурадана // Судебно-медицинская экспертиза. – 2005. – № 3. – С. 27-31.
- Шорманов В.К., Коваленко Е.А., Дурицын Е.П. Определение фурадана в биологических жидкостях // Судебно-медицинская экспертиза. – 2005. – № 5. – С. 36-39.

