Вы здесь
Идентификация и количественное определение фенотерола
Publication in electronic media: 22.10.2011 under http://journal.forens-lit.ru/node/393
Publication in print media: Актуальные вопросы судебной медицины и права, Казань 2010 Вып. 1
ГКУЗ «Республиканское Бюро судебно-медицинской экспертизы МЗ РТ»
Препараты адреностимуляторов по химической структуре напоминают адреналин и отличаются от него тем, что метильный радикал в аминогруппе заменён на другие. Эта замена приводит к тому, что у препаратов появляются новые свойства. Так, изадрин, являющийся изопропилнорадреналином, стимулирует, в основном, β-адренорецепторы и не вызывает повышения артериального давления. Орципреналин, отличающийся от изадрина положением гидроксильных групп при бензольном ядре, также является стимулятором β-адренорецепторов смешанного типа, действует на β1- β2-адренорецепторы, но действует более избирательно на β2-адренорецепторы бронхов, чем сердца, в меньшей степени вызывает тахикардию и снижение артериального давления. Фенотерол по структуре и действию близок к орципреналину, но является более избирательным стимулятором β2-адренорецепторов и оказывает в связи с этим более избирательное, сильное, относительно длительное действие при бронхоспастических состояниях с меньшими побочными явлениями (тахикардия и другие нарушения деятельности сердечно-сосудистой системы) [2].
Фенотерол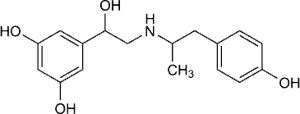
1-(3,5-Диоксифенил)-2-(пара-окси- α -метилфенетиламино)-этанол.
Выпускается в виде гидробромида. Это белый кристаллический порошок. Температура плавления около 230°С, с разложением. Растворимость: 1:10 в воде и 1:11 в этиловом спирте, практически нерастворим в эфире и хлороформе [3].
Фармакологическое действие - бронходилатирующее, токолитическое. Возбуждает β2-адренорецепторы, активирует аденилатциклазу; накапливающаяся цАМФ расслабляет гладкую мускулатуру бронхов, вызывает стабилизацию мембран тучных клеток и базофилов (снижается высвобождение биологически активных веществ), улучшает мукоцилиарный клиренс; обладает токолитическим эффектом.
Имеются указания на то, что препарат оказывает бронхолитическое действие и одновременно усиливает функцию мерцательного эпителия и ускоряет мукоцилиарный транспорт.
Под названием «Беротек» (Германия) препарат применяют для лечения и профилактики бронхиальной астмы, астматического и хронического бронхитов и других бронхолегочных заболеваний, сопровождающихся бронхиолоспазмом.
Специальная лекарственная форма фенотерола (Беротека) в сочетании с холинолитиком ипратропиум-бромидом (атровентом) выпускается в Германии под названием «Беродуал», а препарат, содержащий фенотерол в сочетании с кромолин-натрием, выпускается под названием «Дитэк».
В связи с расслабляющим влиянием на мускулатуру матки, обусловленным стимуляцией β2-адренорецепторов, фенотерол нашёл специальное применение в качестве токолитического средства и выпускается для применения в акушерской практике под названием «Партусистен» [4].
После приёма внутрь фенотерол полностью всасывается из ЖКТ. Интенсивно метаболизируется. Приблизительно 35% от принятой дозы выводится с мочой в течение 24 часов, главным образом в виде неактивных конъюгатов с серной кислотой, в виде неизменённого препарата выводится менее 2%. Примерно 40% от принятой дозы выводится с желчью [5].
Нами было проведено исследование, целью которого было доказательство нахождения фенотерола в секционном материале.
Из обстоятельств дела известно, что гр-ка К., 1937 г.р., страдавшая бронхиальной астмой, была доставлена с места пожара в больницу, где скончалась. Родственники усомнились в правильности лечения, в частности, применялся ли для лечения аэрозоль «Беродуал». В судебно-химическое отделение из отдела экспертиз трупов доставлены: кровь, печень, почка, лёгкое.
В доступной литературе мы не встретили данных о методах изолирования фенотерола. Исходя из физико-химических свойств фенотерола, для изолирования его из биологического материала, были использованы два метода:
- подкисленной водой по Васильевой;
- подкисленным спиртом по Стасу-Отто.
Исследовали искусственную смесь печени с фенотеролом. К навескам по 25 г печени, проверенной на отсутствие лекарственных веществ, добавляли по 1 мг фенотерола, оставляли на 24 часа, после чего изолировали вышеописанными методами. Экстракцию проводили из кислой среды при рН=2,5 смесью хлороформ-эфир 2:1, из аммиачной среды при рН=9,0 хлороформом.
Фенотерол идентифицировали с помощью физико-химических методов анализа: хроматографии в тонком слое сорбента, УФ - спектрофотометрии, газожидкостной хроматографии, хромато-масс-спектрометрии, высокоэффективной жидкостной хроматографии.
Хроматографию в тонком слое сорбента проводили на пластинках «Сорбфил» -ПТСХ-П-А. Использовали следующие системы растворителей: I – метанол; II – хлороформ-ацетон-диоксан-25% аммиак (45:5:47,5:2,5); III – этилацетат-метанол-25% аммиак (17:2:1). Идентификацию проводили в извлечениях из щелочной среды. В извлечениях из кислой среды фенотерол не идентифицирован. В качестве проявителя использовали:
- реактив Драгендорфа (по Мольдаверу);
- 10% раствор хлорида окисного железа;
- 0,1% свежеприготовленный раствор прочного синего Б в 70% растворе этилового спирта;
- реактив Марки.
| Окрашивание с реактивами | Система растворителей | ||
| I | II | III | |
| Значение Rf | 0,57 | 0,48 | 0,46 |
| Реактив Драгендорфа (по Мольдаверу) | оранжевое | оранжевое | оранжевое |
| 10% раствор хлорида окисного железа | сине-фиолетовое | сине-фиолетовое | сине-фиолетовое |
| 0,1% раствор Прочного синего Б в этаноле | фиолетово-розовое | фиолетово-розовое | фиолетово-розовое |
| Реактив Марки | жёлто-зелёное → красно-коричневое | жёлто-зелёное → красно-коричневое | жёлто-зелёное → красно-коричневое |
Для спектрофотометрического исследования использовали извлечения после хроматографической очистки. Снимали спектр поглощения растворов извлечений в 0,1 н растворе соляной кислоты на спектрофотометре НР 8453 фирмы «Хьюлетт-Паккард». В растворе наблюдали максимум поглощения при 275 нм.
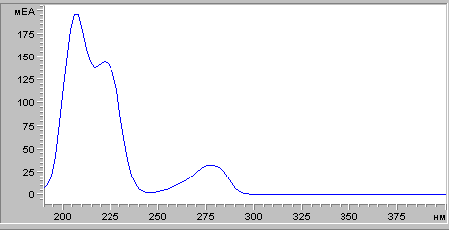
Рис. 1. Спектральная характеристика фенотерола.
Газохроматографическое исследование проводили на хроматографе «Кристаллюкс 4000» с использованием термоионного детектора. Идентификацию проводили на хроматографических колонках с неподвижными фазами, различающимися по полярности: SE-54, OV-17. Ввиду наличия в молекуле фенотерола четырёх гидроксильных групп, в нативном виде он не элюируется с колонки, поэтому мы исследовали фенотерол в виде триметилсилильного производного.
Хромато-масс-спектрометрия. Исследование проводили на хроматогра-фе Agilent 6890 Plus, оборудованном масс-селективным детектором Agilent 5973N и капиллярной колонкой HP-5MS длиной 30 м, внутренним диаметром 0,25 мм и толщиной фазы 0,25 мкм. Время удерживания тетракис - триметилсилильного производного фенотерола 18,52 минут (основные ионы m/z = 322, 236, 207, 356, 412, 323, 179).
Идентификация методом высокоэффективной жидкостной хроматографии проводилась на высокоэффективном жидкостном хроматографе фирмы «Agilent Technologies» 1100 Series методом обращенно-фазной хроматогра-фии на колонке Hypersil ODS 4,0x250 mm 5 micron при температуре 25°С. Подвижная фаза: фосфатный буфер рН 3,3 : ацетонитрил (100:30) [5]. Скорость подвижной фазы 1 мл/мин. Хроматографировали при длине волны 280 нм. Идентификация проводилась по времени и удерживания и УФ-спектру. Время удерживания фенотерола 3,8 минуты.
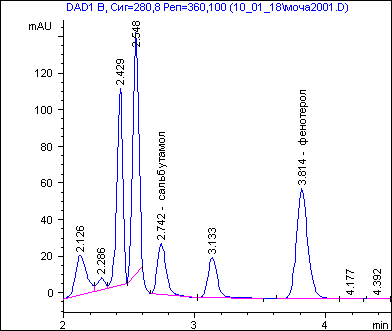
Рис. 2. Хроматограмма экстракта из мочи, содержащей фенотерол.
Количественное определение фенотерола проводилось на высокоэффективном жидкостном хроматографе фирмы «Agilent Technologies» методом внутреннего стандарта. В качестве внутреннего стандарта использовался сальбутамол. Время удерживания внутреннего стандарта 2,7 мин.
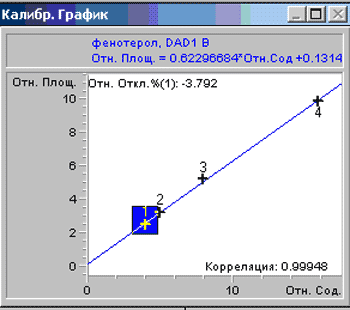
Рис. 3. Калибровочный график определения фенотерола.
Для доказательства наличия фенотерола в экспертном материале использован метод изолирования подкисленной водой с последующей идентификацией в экстрактах из щелочной среды, как описано выше в экспериментальной части. Процент выхода фенотерола при изолировании по данной методике составил 49 - 56 % от введённого количества.
Анализ результатов проведённого исследования позволил нам прийти к следующему заключению.
- При судебно-химических исследованиях целесообразно проводить изолирование фенотерола из биологического материала подкисленной водой, либо подкисленным спиртом с последующей идентификацией в извлечении из щелочной среды.
- Для идентификации фенотерола следует применять комплекс физико-химических методов исследования, включающий хроматографию в тонком слое сорбента, высокоэффективную жидкостную хроматографию, газожидкостную хроматографию, спектрофотометрию в ультрафиолетовой области спектра, хромато-масс-спектрометрию.
- Для количественного определения фенотерола рекомендован метод высокоэффективной жидкостной хроматографии с использованием внутреннего стандарта, т.к. этот метод не требует получения производных фенотерола.
Список литературы
- Высокоэффективная жидкостная хроматография. Теоретические основы и решение прикладных задач. Под редакцией У. Дж. Лоу (колледж здравоохранения Сандерлендского университета) и И. У. Уайнера (кафедра онкологии Мак-Гиллского университета, Монреаль).
- Машковский М.Д. Лекарственные средства. Справочник. – М.: «Новая волна», 2006.
- Спецификация на препарат «Беротек дозированный аэрозоль» фирмы «Берингер Ингельхайм» Германия. НД 42-10244-99. Фармакопейный государственный комитет/ Министерство здравоохранения РФ.
- Справочник ВИДАЛЬ. Лекарственные препараты в России. – 1996.
- Clarke s Isolation and identification of drugs in pharmaceuticals, Body fluids, аnd post-mortem material. – London, 1986.

