Вы здесь
Идентификация ацетальдегида в биологических объектах газохромато-графическим методом
Publication in electronic media: 22.10.2011 under http://journal.forens-lit.ru/node/392
Publication in print media: Актуальные вопросы судебной медицины и права, Казань 2010 Вып. 1
ГКУЗ «Республиканское бюро судебно-медицинской экспертизы МЗ РТ»
Судебно-медицинская диагностика причины смерти в случаях алкогольной интоксикации нередко вызывает серьезные затруднения. Это, в первую очередь, относится к тем случаям, когда отсутствуют достаточно выраженные изменения внутренних органов, а концентрация этанола в крови либо незначительна, либо он вообще не обнаруживается. В подобных ситуациях объективным доказательством алкогольной интоксикации может служить обнаружение продуктов окисления этанола, в частности ацетальдегида, так как он служит одной из причин похмельного состояния, долго сохраняясь в организме [3].
Ацетальдегид (АЦ) – уксусный альдегид, органическое соединение, легко летучая бесцветная жидкость с удушающим запахом, смешивается во всех отношениях с водой, спиртом, эфиром. АЦ обладает всеми типичными свойствами альдегидов. В присутствии минеральных кислот он полимеризуется в жидкий тримерный паральдегид и тетрамерный метальдегид. Пары тяжелее воздуха, на воздухе окисляется с образованием перекисей. При разбавлении водой приобретает фруктовый запах. Применяют в огромных масштабах в производстве уксусной кислоты, уксусного ангидрида, различных фармацевтических препаратов и т.д. [2].
В организме человека постоянно присутствует эндогенный этанол, образующийся в биохимических процессах. Источник эндогенного этанола – эндогенный ацетальдегид, являющийся продуктом углеводного обмена, который образуется, главным образом, в результате декарбоксилирования пирувата при участии соответствующего фермента пируватдегидрогеназного комплекса. По литературным данным концентрация эндогенного этанола в крови здоровых людей в среднем составляет 0,0004 г/л; максимальные значения не превышают сотых долей г/л, концентрация эндогенного ацетальдегида в 100-1000 раз меньше. АЦ является основным промежуточным метаболитом этанола. Основной путь – с участием алкогольдегидрогеназы по схеме:
С2Н5ОН + NAD+ ↔ СН3СНО + NADH + H+.
Образующийся АЦ окисляется альдегиддегидрогеназой (АДГ) до ацетата [5]. В течение 1 часа в организме человека может быть метаболизировано 7- 10 г алкоголя, что соответствует снижению его концентрации в среднем на 0,1-0,16‰. Окислительные процессы могут активироваться и достигать 0,27‰/ч. Длительность токсикодинамики определяется, в первую очередь, количеством принятого алкоголя. При приеме больших количеств АЦ может сохраняться в организме 1 сутки и дольше. В течение 1-2 ч после взятия крови у живых лиц ферментативное окисление алкоголя прекращается, равно как и после наступления смерти в крови трупов [1]. Основным местом образования АЦ из этанола и последующего его окисления является печень. Поэтому наибольшее количество ацетальдегида в опытах определяли в печени, затем в крови, наименьшее – в цереброспинальной жидкости.
Идентификацию АЦ в биологических объектах проводили на газовом хроматографе «Кристаллюкс-4000М», снабженном компьютерной программой «NetchromWin», пламенно-ионизационным детектором на капиллярных колонках. Использовались три капиллярные колонки:
- колонка №1 30м/0,53 мм/1,0µ, ZB – WAX (Polyethylen Glycol);
- колонка №2 30м/0,32 мм/0,5µ, ZB – 5 (5% Penyl methyl polysiloxane);
- колонка №3 50 м/0,32 мм/0,5µ, HP – FFAP.
Температура колонок 50 °С, температура детектора 200 °С, температура испарителя 200 °С. Скорость потока газа-носителя (азота) 30 мл/мин, воздуха 500 мл/мин, водорода 60 мл/мин.
Отмечали хорошее разделение смеси (рис. 1): ацетальдегид+диэтиловый эфир+ацетон+этилацетат+этанол+ацетонитрил.
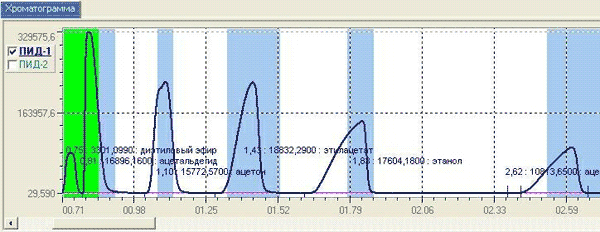
Рис. 1. Распределение веществ.
Обнаружению и определению ацетальдегида (табл. 1) не мешают ацетон, метанол, этанол и другие алифатические спирты, этилацетат, хлорорганические соединения, ароматические углеводороды, диэтиловый эфир.
Таблица 1. Сравнительные результаты идентификации ацетальдегид в смеси с другими веществами
| Анализируемое вещество | Колонка №1 | Колонка №2 | Колонка №3 |
| Диэтиловый эфир | 44 с | 2 мин 22 с | 5 мин 41 с |
| Ацетальдегид | 49 с | 2 мин 04 с | 6 мин 06 с |
| Ацетон | 1 мин 10 с | 2 мин 20 с | 7 мин 10 с |
| Этилацетат | 1 мин 43 с | 3 мин 14 с | 8 мин 24 с |
| Этанол | 2 мин 49 с | 2 мин 11 с | 9 мин 32 с |
| Ацетонитрил | 2 мин 52 с | 2 мин 21 с | 12 мин 57с |
Колонку №3 HP – FFAP не использовали для количественного анализа, так как такой анализ требует больших временных и экономических затрат.
Построение калибровочного графика ацетальдегида. Для построения ка-либровочного графика использовались водные растворы ацетальдегида (х.ч. для хроматографии) с концентрацией 1,5; 15; 30; 60; 150 мг/л. В качестве внутреннего стандарта – водный раствор ацетонитрила с концентрацией 78 мг/л.
Методика исследования: во флакон из стеклодрота, содержащий 0,5 мл 50% раствора фосфорно-вольфрамовой кислоты, помещали 0,5 мл внутреннего стандарта – раствор ацетонитрила с концентрацией 78 мг/л и 0,5 мл раствора ацетальдегида с известной концентрацией. Для уменьшения парциального давления паров воды к смеси добавляли 2 г безводного сульфата натрия. Флакон закрывали резиновой пробкой, фиксировали металлическим зажимом, нагревали в кипящей водяной бане в течение 5 минут и 0,5 мл тёплой парогазовой фазы вводили в испаритель хроматографа. Производили расчёт фактора чувствительности (табл. 2) для 2-х колонок:
Таблица 2. Расчёт фактора чувствительности
| Аац, мг/л | Колонка № 1 | Колонка № 2 | ||
| Sх, в мв/мин | Sст, в мв/мин | Sх, в мв/мин | Sст, в мв/мин | |
| 150 | 69 | 10 | 15 | 2 |
| 60 | 39 | 11 | 4.5 | 1.7 |
| 30 | 24 | 14 | 3 | 2 |
| 15 | 10 | 12 | 1.2 | 1.5 |
| 1,5 | 1.2 | 15 | 0.18 | 2 |
Обозначения: Аац – концентрация ацетальдегида; Sх – площадь пика ацетальдегида; Sст – площадь пика ацетонитрила.
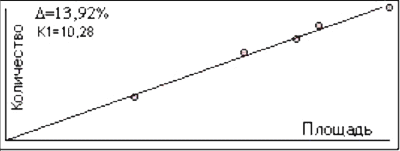
Рис. 2. График зависимости отношения площадей от концентраций ацетальдегида для 1-ой колонки.
По вышеописанной методике проводили исследования из биологических объектов (кровь, моча, вещество головного мозга, печень, почка и др.).
Исследовано 40 случаев при подозрении на отравление «суррогатами алкоголя». Результаты исследования этих случаев сведены в таблицу 3.
Таблица 3. Распределение этанола
| Отсутствие АЦ и этанола | Обнаружение АЦ до 1 мг/л и этанол менее 0,3‰ | Обнаружение АЦ 1-10 мг/л и этанола 0,3‰-6‰ | Обнаружение АЦ 30 мг/л и отсутствие этанола | |
| 15% из них: | 25% | 55% | 5% | |
| 83% из ЛПУ | 17% скоропостижная смерть | |||
Случай из практики: доставлен труп мужчины 40 лет из реанимационного отделения. В стационаре больной находился 4 часа, в анамнезе для лечения использован «Эспераль». В процессе судебно-химического исследования биологических объектов дисульфирам и другие лекарственные вещества не обнаружены. В крови этиловый алкоголь не обнаружен. Обнаружен АЦ с концентрацией: 0,5 мг/л в крови, 28 мг/л в желудке, 2 мг/л в печени, 1 мг/л в почке, 29 мг/л в кишечнике.
При одновременном употреблении этилового алкоголя и дисульфирама (тетурам) образуется АЦ. Механизм заключается в том, что дисульфирам ингибирует фермент алкогольдегидрогеназу, задерживая окисление этанола на уровне АЦ, что приводит к интоксикации организма человека. Некоторые лекарственные препараты могут оказывать тетурамоподобную активность, вызывая непереносимость к алкоголю. Это, прежде всего, хлорпропамид и другие противодиабетические сульфаниламидные препараты, метронидазол и т.п., производные нитро-5- имидозола, бутадион, антибиотики [4].
Выводы
- Использован современный высокочувствительный газовый хромато-граф «Кристаллюкс-4000М» с детектором ДИП и компьютерной программой «NetchromWin», который позволяет определять малые концентрации АЦ, близкие к эндогенным.
- Предложены новые селективные, высокочувствительные капиллярные колонки с фазами ZB-WAX, ZB-5, позволяющие обнаружить до 100 мкг (0,001%о) ацетальдегида в исследуемых пробах.
- Подобраны оптимальные условия, позволяющие проводить газо-хроматографический скрининг ацетальдегида и следующих органических растворителей: алифатических спиртов, хлорорганических растворителей, ароматических углеводородов, этилацетата, ацетона и диэтилового эфира в течение 15 минут.
- Рекомендовано проводить количественное определение как этанола, так и ацетальдегида при диагнозе «алкогольная интоксикация».
Список литературы
- Альберт А.// Избирательная токсичность. – М., 1989. – Т.1 – С. 213.
- Моррисон Р., Бойд Р.// Органическая химия, пер. с англ.-1974-78гг
- Савич В.И., Валладарес Х. АГусаков., Ю.А., Скачков З.М. // Суд.-мед. эксперт. – 1990. – № 4. – С. 24-27.
- Успенский А.Е., Листвина В.П.// Фармакол. и токсикол. – 1984. – №1. – С. 119-122.
- Шитов Л.Н.Методы исследования и токсикология этилового алкоголя (химико-токсикологическая лаборатория ЯОКНБ). – 2007.

