Вы здесь
Способ уменьшения влияния некоторых мешающих факторов при определении карбоксигемоглобина в гнилостной крови по методу Букиной и Ушаковой
Publication in electronic media: 11.06.2009 under http://journal.forens-lit.ru/node/76
Publication in print media: Актуальные вопросы судебной медицины и экспертной практики, Барнаул-Новосибирск 2008 Вып. 14
П. В. Никитин
г. Кемерово
Наиболее распространенные методы обнаружения и количественного определения карбоксигемоглобина в крови основаны на спектрофотомерии в видимой области спектра. Все спектрофотометрические методы очень требовательны к прозрачности исследуемых растворов, Поэтому разными авторами предлагались свои гемолизирующие растворы – разнообразные буферные системы, разбавленные растворы едкого натра и аммиака, а также, при необходимости, предлагалось фильтрование или центрифугирование гемолизатов. В некоторых случаях, даже при исследовании визуально прозрачных растворов, получаются недостаточно достоверные результаты. Это может быть связано, по нашему мнению, с присутствием в растворе «третьих» оптически активных веществ, помимо двух компонентов, учитываемых при градуировке (т.е. карбоксигемоглобина и гемоглобина).
При исследовании некоторых гнилостно измененных (либо высохших) образцов крови, получающиеся при добавлении дитионита натрия, спектры являются искаженными: четко выраженный максимум при 558 (560) нм и значительно менее выраженный – «ступенькой» – в области около 530 нм, что не соответствует спектрам восстановленного гемоглобина или карбоксигемоглобина. Получаемые спектры не подходят под обычную качественную интерпретацию в рамках двухкомпонентной модели, а результаты расчета концентрации карбоксигемоглобина по та-ким спектрам (по предложенному нами ранее «расширенному» варианту метода Букиной и Ушаковой) имеют столь большие среднеквадратичные отклонения, что это не позволяет использовать результаты даже в качестве ориентировочных. Фильтрование, как и центрифугирование растворов крови в 0,1% растворе аммиака в таких случаях являются малоэффектив-ными.
Мы предположили, что данное искажение спектров объясняется присутствием в исследуемой крови другого деривата гемоглобина, а именно, гематина. Возможно, он образуется вследствие ощелачивания крови при гниении (из-за образования аммиака и аминов), либо его присутствие в некоторых образцах крови связано с прижизненными процессами (массированный распад эритроцитов при тяжелых ожогах и т.д.). Этот дериват гемоглобина растворим в щелочах, а при добавлении восстановителя – дитионита натрия – реагирует с глобином с образованием гемохромогена. Спектральные характеристики гемохромогена, описанные в литературе (Туманов А.К., 1961), совпадали с наблюдаемыми нами в подобных случаях. Гематин и гемохромоген нерастворимы в воде; именно это свойство мы и предложили для «улучшения» спектров растворов крови. Кровь разводится водой (в соотношении приблизительно 1:5-1:10), фильтруется через плотный бумажный фильтр, а затем уже прозрачный водный фильтрат-«концентрат» доводится до необходимой оптической плотности (до общего разведения 1:100-1:200) 0,1% раствором аммиака. В некоторых случаях лучшие результаты получались при первоначальном разведении крови в слабом (0,1%) водном растворе уксусной кислоты. Получаемые спектры вполне пригодны для качественной и количественной интерпретации, а результаты расчетов лучше соответствуют результатам газовой хроматографии, цветных реакций, независимому количественному определению по методу Фрейтвурста-Майнеке.
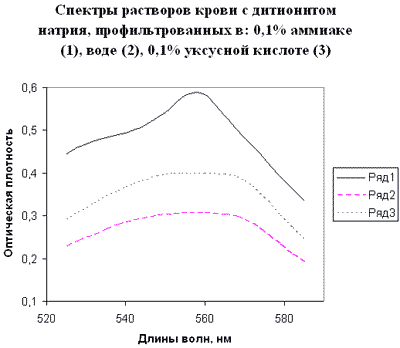
Для иллюстрации приводим реальный экспертный случай - спектры растворов одной и той же гнилостно измененной крови после добавления дитионита натрия. Результаты расчета концентрации карбоксигемоглобина (среднее значение по шести формулам «расширенного» метода Букиной и Ушаковой): спектр 1 – 13% (относительное среднеквадратичное отклонение этого среднего значения – 158%!), спектр нетипичный и не поддающийся качественной интерпретации в рамках этого метода; спектр 2 – 24% (отн. СКО – 28%); спектр 3 – 25% (отн. СКО – 21%); последние спектры типичны для невысокой концентрации карбоксигемоглобина, с большим, но уже вполне приемлемым разбросом результатов определения.